二萜生物碱类化合物紫杉醇的抗疟活性及协同抗耐药机制研究
恶性疟原虫对青蒿素类药物的耐药性(ART-R)随K13基因突变(如C580Y、R539T) 扩散日益严峻,显著增加治疗失败风险,严重威胁全球疟疾消除目标。传统抗疟新药研发周期长、成本高,且多数候选药物沿用单一作用机制,易诱导交叉耐药性;现有药物多聚焦寄生虫代谢或血红蛋白降解途径,针对细胞骨架动力学的研发相对滞后。我们前期研究发现,生物碱类药物可通过显著干扰疟原虫生长发育进程、抑制其红内期正常增殖循环,发挥明确抗疟活性(Microorganisms, 2025)。我们在后续研究中偶然发现,同为生物碱类化合物的抗肿瘤药物紫杉醇(Paclitaxel, PTX),同样具备强效抑制疟原虫生长发育的潜力。紫杉醇最早从红豆杉树皮中提取获得,长期广泛应用于临床癌症化疗,尽管早期已有研究提示其可能存在抗疟活性,但针对青蒿素耐药株的具体抑制效力、及其核心作用靶点,以及与青蒿素联用是否能产生协同抗疟效应等关键科学问题,长期缺乏系统性机制解析与体内试验验证,限制了其在抗疟领域的进一步开发与应用。
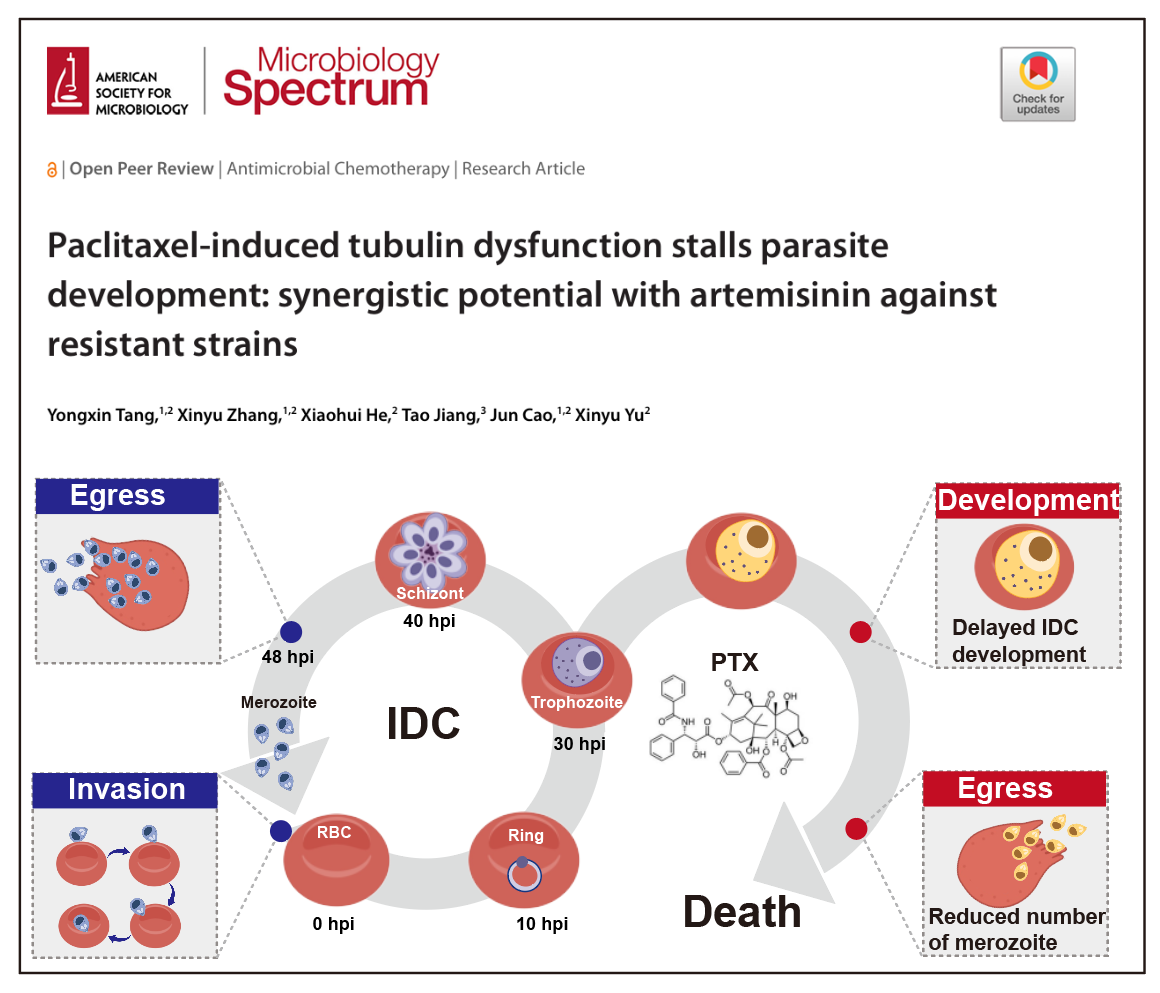
2026年4月30日,江苏省血吸虫病防治研究所俞心愉/中国科学院生物物理所江涛课题组合作在美国微生物学会旗下Microbiology Spectrum期刊(JCR-Q2, IF:3.8)上发表了题为“Paclitaxel-Induced Tubulin Dysfunction Stalls Parasite Development: Synergistic Potential with Artemisinin against Resistant Strains”的研究性论著。研究结果表明,体外实验中紫杉醇(PTX)对恶性疟原虫野生型虫株及青蒿素抗性虫株均表现出良好抑制活性;进一步机制分析显示,PTX可特异性导致疟原虫裂殖体期核分裂异常,显著减少子代裂殖子生成量。在针对青蒿素耐药株的环状体生存试验中,PTX与双氢青蒿素(DHA)联用呈现显著协同效应,能有效阻断耐药寄生虫通过休眠机制逃避药物杀伤的关键路径。体内实验结果进一步明确,PTX与DHA联合用药时,展现出协同抗疟优势:不仅能显著增强对青蒿素耐药虫株的清除效果,有效降低停药后寄生虫再燃风险,还能显著提升感染耐药株小鼠的存活率,直接证实PTX具备作为抗疟配伍药物的良好应用潜力。值得关注的是,研究还发现PTX对疟原虫配子体具有显著杀伤活性,可使成熟配子体数量显著减少,这一特性为阻断疟疾传播提供了额外优势,进一步凸显其在抗疟联合疗法中的应用价值。
PTX作为临床常用化疗药物,其固有的细胞毒性较大这一不足,限制了其直接用于抗疟临床治疗。而本研究的相关发现,不仅为后续基于PTX的结构修饰研究提供了明确方向,更为通过分子改造实现其抗疟活性优化、降低细胞毒性的药物研发工作提供了关键实验依据,同时也为开展PTX与其他抗疟药物的联用策略探索、作用机制深化解析等后续研究奠定了坚实基础。
南京医科大学研究生唐永鑫、张欣宇,江苏省血吸虫病防治研究所何晓辉为本文共同第一作者;江苏省血吸虫病防治研究所俞心愉副研究员、曹俊研究员,中国科学院生物物理所江涛研究员为本文共同通讯作者。原文链接:Paclitaxel-Induced Tubulin Dysfunction Stalls Parasite Development: Synergistic Potential with Artemisinin against Resistant Strains
最近新闻
-
2026.05.26
-
2026.05.06
-
2026.04.13
-
2026.03.26
-
2026.03.24
-
2026.03.19
-
2026.03.09
-
2026.01.20
-
2026.01.19
-
2025.12.24









